Nessun prodotto nel carrello.
Menu
Usa le tue credenziali per accedere
Compila il form sottostante per creare il tuo account
* campi obbligatori
Registrati
Menu


La relazione tra luce e colore

La relazione tra luce e colore
Per parlare di fotometria e per capire come si misura l'intensita della luce, bisogna dapprima capire la relazione tra colore e luce.
I colori dipendono dalla luce e quello che noi vediamo come colore deriva dall’effetto della luce su un oggetto. Quando un fascio di luce bianca colpisce un oggetto, questo può essere riflesso, assorbito o trasmesso. Il vetro trasmette gran parte della luce con cui entra in contatto, perciò appare incolore. Un esempio è la neve che riflette tutta la luce e per questo appare bianca. Al contrario di un vestito nero che assorbe tutta la luce e quindi appare nero. La maggior parte degli oggetti appare colorata parchè la loro struttura chimica assorbe alcu-ne lunghezze d’onda di luce e ne riflette altre.
Per questo quando parliamo di luce, di solito ci riferiamo alla luce bianca. Una linea sottile di luce è chiamata raggio; un fascio invece è costituito da molti raggi di luce. Quando la luce bianca passa attraverso un prisma (un oggetto triangolare trasparente) i colori che compongono la luce bianca si disperdono in sette bande di colore (fasci di luce), che formano lo spettro. Sette colori costituiscono la luce bianca: rosso, arancione, giallo, verde, blu, indaco e viola. In qualsiasi spettro, i fasci di colore sono sempre organizzati in questo ordine da sinistra verso destra.
Le sostanze hanno la capacità intrinseca di assorbire la luce con un particolare colore. Supponendo di orientare un fascio di luce bianca verso una sostanza che assorbe la luce blu si verificherà una trasmissione di luce di colore giallo, il colore complementare del blu. Questa luce gialla raggiunge i nostri occhi e di conseguenza vediamo la sostanza colorata di giallo.
L’analisi colorimetrica si basa sulla variazione di colore che avviene nel campione in analisi. Questo cambiamento di colore è direttamente legato alla concentrazione della sostanza da ricercare.

Colorimetria

Colorimetria
La colorimetria è in parole semplici la misura del colore. Ovvero la determinazione della concentrazione di una sostanza attraverso la misura dell’assorbimento della luce relativa ad essa. In colorimetria una luce bianca, naturale o artificiale, è utilizzata come sorgente del sistema ottico e le analisi vengono effettuate con uno strumento chiamato colorimetro o fotometro.
Un’analisi colorimetrica si basa sul principio che molte sostanze reagendo con un composto chimico producono un cambiamento di colore che sarà proporzionale alla concentrazione della sostanza da misurare. Quando una sostanza è esposta ad un fascio di luce di intensità (I0) una parte della radiazione è assorbita dalla sostanza, emettendo una radiazione di intensità (I). La differenza di intensità è utilizzata per la determinazione colorimetrica.
L’assorbanza è data anche da: A= ελ * C * l
dove:
A è un numero adimensionale (senza unità di misura)
ελ è la costante di proporzionalità, detto coefficiente di estinzione molare; è una costante per una determinata sostanza, a condizione che la temperatura e la lunghezza d’onda siano costanti [L/(mol*cm)]
C è la concentrazione della sostanza (moli/litro)
l definito cammino ottico, ovvero la distanza che percorre il fascio di luce che attraversa il campione (cm)
Tuttavia, conoscendo i fattori noti, la concentrazione (C) può essere calcolata a partire dall’assorbanza della sostanza in relazione alla radiazione emessa (I).
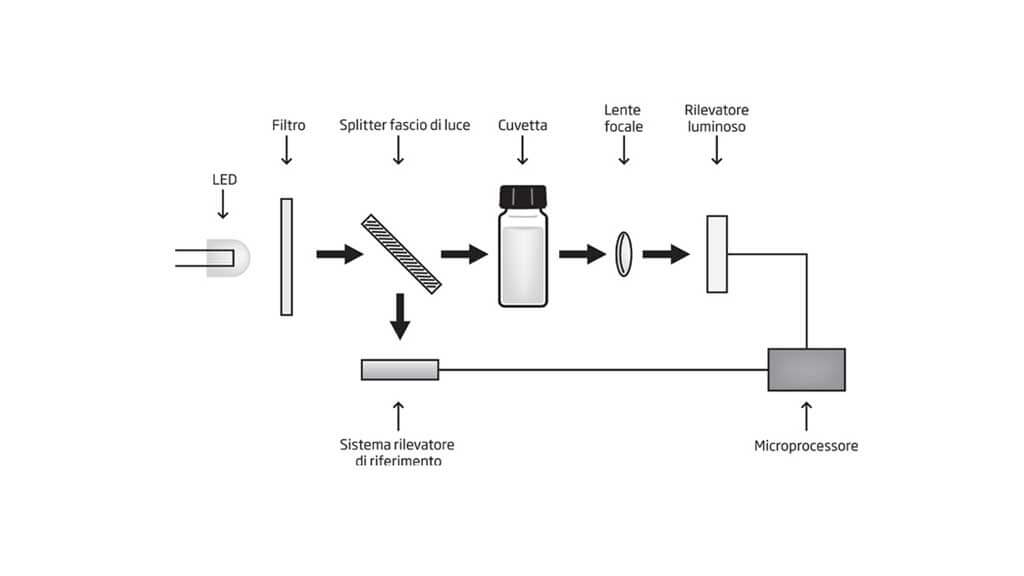
Schema ottico fotometrico

Schema ottico fotometrico
Nella figura, è possibile vedere un tipo schema di sistema ottico fotometrico, utilizzato dai fotometri multiparametro Serie HI833xx e dai fotometri portatili HANNA
Sorgente luminosa (LED o Lampada a Tungsteno)
Rispetto al tungsteno, i LED garantiscono prestazioni più elevate: massima efficienza luminosa, basso consumo energetico, lunga durata, minima emissione di calore.
Filtri di interferenza a banda stretta
I filtri di interferenza di elevata qualità, con una banda larga appena 8 nm, filtrano la luce in modo molto selettivo, e garantiscono accuratezza ± 1nm della lunghezza d’onda. Questa maggiore efficienza si traduce in una sorgente luminosa forte e brillante, con una maggiore stabilità del segnale
Rilevatore di riferimento per luce stabile
I fotometri Serie HI833xx sono dotati di uno splitter del fascio di luce e un rilevatore di riferimento che compensa le fluttuazioni della sorgente luminosa, dovute a variazioni di tensione di alimentazione o della temperatura ambientale.
Cammino ottico
Utilizzando cuvette in vetro con diametro più ampio (25 mm), si aumenta il cammino ottico della luce, consentendo così una rilevazione di valori di assorbanza più elevati e di conseguenza una maggiore precisione anche a basse concentrazioni.
Lente di messa a fuoco
La lente consente di raccogliere tutta la luce che fuoriesce dalla cuvetta e di focalizzarla sul fotorilevatore al silicio, eliminando così gli errori dovuti ad imperfezioni e graffi presenti nella cuvetta di vetro.

Esempio: supponiamo che per una sostanza chimica esiste un’assorbanza massima di 610 nm, di seguito è riportato un esempio di come funzionano i colorimetri per determinare la concentrazione

Esempio: supponiamo che per una sostanza chimica esiste un’assorbanza massima di 610 nm, di seguito è riportato un esempio di come funzionano i colorimetri per determinare la concentrazione
Lampada al tungsteno: Lampada incandescente con un filamento al tungsteno
LED: Diodo ad Emissione di Luce
Il cammino ottico è misurato mediante la grandezza della cuvetta contenente il campione. La cella fotometrica raccoglie la radiazione (I) emessa dal campione e la converte in corrente elettrica, producendo un potenziale in mV. Il microprocessore utilizza questo potenziale per convertire il valore in uscita in concentrazione, nell’unità di misura desiderata e lo visualizza sul display. Il campione da analizzare viene trattato seguendo una procedura ben definita e un software pre-programmato all’interno dello strumento assicura l’utilizzo di una curva di calibrazione relativa al metodo. Questa curva è utilizzata come riferimento per ogni misurazione.
Un esempio di analisi colorimetrica è il metodo Nessler per l’ammoniaca, che è stato proposto per la prima volta nel 1856. Nessler ha scoperto che aggiungendo una soluzione alcalina di Hgl2 e Kl ad una soluzione diluita di ammoniaca si produce una colorazione marrone/gialla con in¬tensità di colore proporzionale alla concentrazione di ammoniaca presente nel campione in analisi. Una quantità di campione o di soluzione standard è stata trasferita in una fiala (cuvetta) in vetro (con fondo piano). Le cuvette sono state poi posizionate in una griglia dotata di una superficie riflettente sul fondo che permette alla luce di passare attraverso la soluzione e la cuvetta. I colori dei campioni sono stati confron¬tati con quelli delle soluzioni standard per determinare la concentrazione del campione non noto. Una forma modificata di questo metodo è utilizzata per l’analisi di am¬moniaca nelle acque di scarico.